Réparer le corps humain. Une quête vers l’immortalité?
Disposer pour chaque individu d’une source illimitée de cellules souches pluripotentes capables de réparer tissus et organes endommagés ou vieillissants.
Bernard Klein

Je me souviens d’un stage de yoga en 2012 au Maroc. Le formateur évoquait une certitude, nous sommes tous mortels ou pour reprendre une assertion classique, tout être humain est atteint d’une maladie mortelle, la vie.
Je mentionnais alors les récents travaux remarquables1 de l’équipe Japonaise du Pr Yamanaka montrant que les cellules d’un individu adulte pouvaient être reprogrammées en cellules souches identiques à celles présentes aux premiers jours de la vie d’un embryon. Cellules souches capables de générer toutes les cellules, tissus et organes d’un individu : sang, intestin, peau, foie, os, cartilage, cerveau, cellules sexuelles, etc… Voir «Pour aller plus loin… » ci-dessous.
S’est enclenchée une discussion sur l’intérêt de réparer un corps vieillissant, dans une planète bien surpeuplée, discussion philosophique ouverte.
En résumé, ces chercheurs ont trouvé une clef permettant d’ouvrir une serrure cachée présente dans nos cellules qui enclenche leur reprogrammation en cellules souches de type embryonnaire. Fait remarquable, cette clef est simple par rapport à la complexité d’un corps humain. Ces cellules reprogrammées sont capables de prolifération illimitée, se divisant en deux cellules filles identiques à elles mêmes, pendant des années dans des boîtes de culture en laboratoire. En changeant les conditions de culture, elles peuvent générer chacun des 220 types cellulaires constituant les tissus et organes de notre corps. Pour cette raison, elles sont appelées cellules souches pluripotentes. Du fait de la simplicité de cette clef de reprogrammation, ces travaux ont été rapidement confirmés et amplifiés par un grand nombre d’équipes mondiales, en particulier en améliorant la clef ouvrant cette serrure cachée. En combinant ces clefs, le Dr Lemaitre a montré la possibilité d’effacer cent ans de vieillissement et de reprogrammer des cellules de sujets centenaires en cellules souches avec des propriétés identiques à celles présentes aux premiers jours de leurs vies embryonnaires2.
Cette découverte apportait une telle révolution conceptuelle que ces scientifiques ont reçu le prix Nobel en 2012, cinq ans après la publication de leurs travaux.
Comme illustré dans le schéma ci-dessous, vous comprenez que ces travaux ouvrent la voie à disposer pour chaque individu d’une source illimitée de cellules souches pluripotentes capables de réparer des tissus et organes endommagés ou vieillissants. Cependant, de la levée de ce verrou conceptuel à des applications thérapeutiques sécurisées, la route est longue, nécessitant une série d’améliorations technologiques. Les premiers essais thérapeutiques utilisant ces cellules reprogrammées ont débuté3.
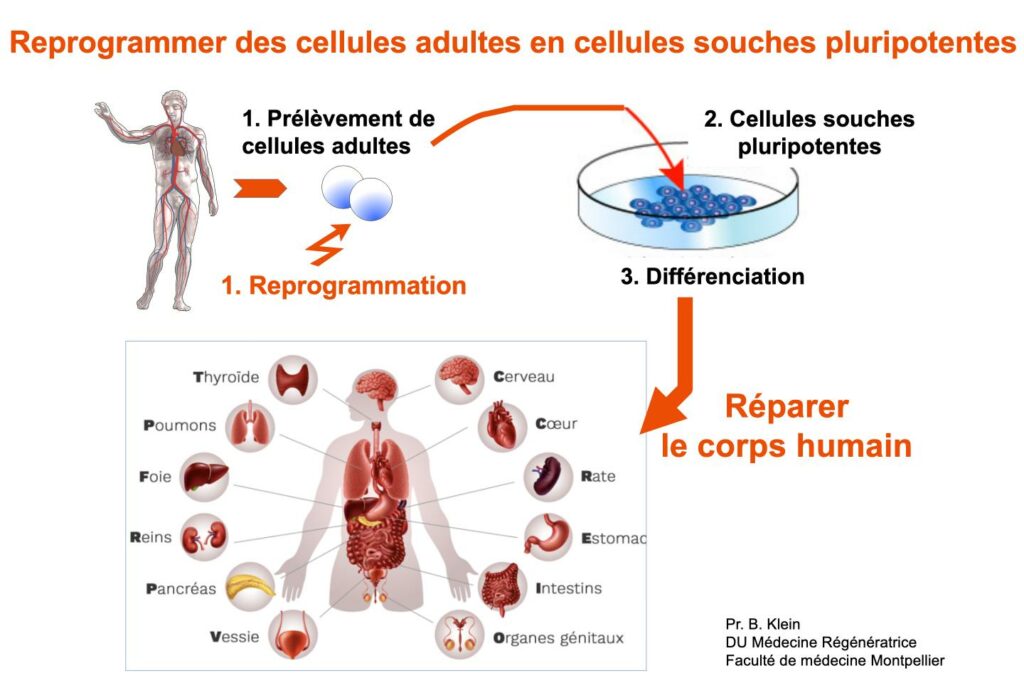
Quel peut être l’intérêt de donner un aperçu de ces recherches à des pratiquants de yoga ? Pour moi la pratique de yoga passe par une perception de notre interconnexion constante avec l’Univers, en particulier avec la multitude des organismes vivant en symbiose avec nous. Rappelons que nous venons de bactéries qui après un long processus d’évolution de 4 milliards d’années ont généré des êtres de plus en plus sophistiqués, dont nous-mêmes. Et les travaux mentionnés ci-dessus nous apprennent que nous avons gardé au coeur de nos cellules ce potentiel d’immortalité qu’ont les bactéries et certains organismes multi-cellulaires. Prendre conscience de ce potentiel, prendre conscience que par notre action quotidienne – activité physique, alimentation, pratique de yoga, méditation, maîtrise du stress – nous pouvons influencer positivement ou négativement des mécanismes sous-jacents à ce potentiel d’immortalité, ne peut que nous renforcer dans la nécessité de prendre du recul, d’approfondir nos connaissances sur cet Univers fantastique, sur la richesse et la fragilité de la vie sur terre. Dans un article récent publié par notre association, Christine Chaput nous montre la profondeur de la connaissance de l’être humain par les yogis. Elle indique « La science des yogis ne nous arrive en occident que de manière très parcellaire, mais cette science expérimentale, subtile et millénaire mériterait un rapprochement avec la science moderne au bénéfice de tous ». C’est ce que notre association essaye de faire à son modeste niveau au travers de ces Regards sur la science.
Dans la suite de cet article, je vous donne un bref aperçu d’un livre récent « Guérir la vieillesse » de JM Lemaitre qui fait le point des avancées scientifiques et médicales sur cette thématique. Pour les passionnés, je recommande ce livre complet, érudit. La plupart des chapitres, reprenant des concepts déjà vulgarisés, sont faciles d’abord. D’autres chapitres faisant la synthèse de travaux scientifiques récents sont plus ardus.
Puis profitant d’une série de cours grand public sur la médecine régénératrice que j’avais donnée aux associations de malades à la demande de l’INSERM, j’écrirai cette année quelques articles vous livrant un aperçu simple des principales perpectives thérapeutiques dans ce domaine fascinant. Dans le paragraphe ci-dessous « Pour aller plus loin… », je débute par les cellules qui sont à la source de notre vie, les cellules souches embryonnaires, puis les cellules souches adultes.
« Guérir la vieillesse ». Jean Marc Lemaitre. Editions HUMENSCIENCES, 2022.
La première partie de ce livre (100 pages) est intitulée « Pourquoi vieillissons-nous ? ».
Le chapitre 1, facile à lire, est une revue des différentes théories du vieillissement, des premiers philosophes/médecins Grecs aux temps contemporains. Il aurait été intéressant de s’ouvrir aux cultures asiatiques ou arabes. Nous y reviendrons probablement dans un autre article. Le chapitre 2, assez complexe pour un profane, explique les mécanismes impliqués dans le vieillissement. Le chapitre 3 résume les avancées récentes pour évaluer l’âge biologique d’un individu, notamment à l’aide de marqueurs récemment identifiés de la plasticité de notre génome. Et vous ne serez pas surpris par ce passage du livre :
En suivant ces marques, une étude pilote de huit semaines, menée sur 43 adultes entre 50 et 72 ans, a montré qu’un style de vie contrôlé (alimentation, sommeil, activité et compléments alimentaires) aboutissait à un âge de 3,2 années plus jeune que celui mesuré huit semaines auparavant, c’est-à-dire avant la mise en place du programme. À l’opposé, la consommation de tabac induit des changements de profil de méthylation des gènes associés aux maladies cardiovasculaires et au cancer.
JM Lemaitre, Guérir le vieillesse
Le chapitre 4, de lecture aisée, rappelle qu’une relative immortalité est déjà observée pour des espèces végétales ou animales dans la nature et résume les avancées scientifiques récentes pour en comprendre les mécanismes. Le végétal le plus ancien répertorié à présent est un herbier de posidonie dans les îles Baléares en Méditerranée avec un âge estimé entre 80000 et 200000 ans4.
La partie 2 de 130 pages « Que nous est-il permis d’espérer ? » aborde les perspectives thérapeutiques.
Le chapitre 5, fait une revue des cellules souches adultes puis de l’utilisation potentielle des cellules souches pluripotentes. Je reprends sous une forme abrégée les points essentiels dans le paragraphe ci-dessous « Pour aller plus loin… ». Le chapitre 6, facile à lire, fait l’état des lieux des stratégies pour retarder le vieillissement : entre autres, une activité physique constante, une restriction calorifique. Les milliardaires de la Silicon Valley investissent massivement pour limiter le vieillissement, probablement de façon désintéressée (?). Citons ce passage du livre:
« Le milliardaire américain Peter Thiel, cofondateur de PayPal, se montre très intéressé par la recherche sur le vieillissement. Il a notamment donné 3,5 millions de dollars à la fondation Methuselah (Mathusalem) afin de promouvoir celle-ci. En 2016, il témoignait publiquement de son intérêt pour la parabiose, une technique consistant à relier deux organismes afin d’établir entre eux une seule et même circulation sanguine : « Je ne suis pas convaincu que l’on ait trouvé la panacée qui marche vraiment […] Je regarde du côté de la parabiose, que je trouve très intéressante. Dans les années 1950, on a injecté du plasma issu du sang de souris jeunes dans celui des souris âgées et ils ont trouvé qu’il y avait un effet de rajeunissement massif […] Puis on a laissé tomber ces travaux. Je pense qu’il y a beaucoup de choses qui ont été étrangement inexplorées. »
JM Lemaitre. Guérir la vieillesse
Pour aller plus loin…
Au commencement de la vie, des cellules souches totipotentes puis pluripotentes.
Nous provenons tous d’un œuf, résultat de la fécondation d’un ovocyte de notre mère par un spermatozoïde de notre père (jour 0). Cet œuf entame un processus rapide de prolifération et division cellulaire pour générer un embryon précoce de 16-32 cellules au jour 4. A ce stade, cet embryon précoce est composé de cellules souches dites totipotentes, car toutes capables si elles sont implantées dans un utérus de pénétrer la paroi utérine et former un fœtus puis un nouveau-né. Ce sont ces embryons précoces qui sont générés dans les laboratoires de fécondation in vitro en cas d’infertilité.
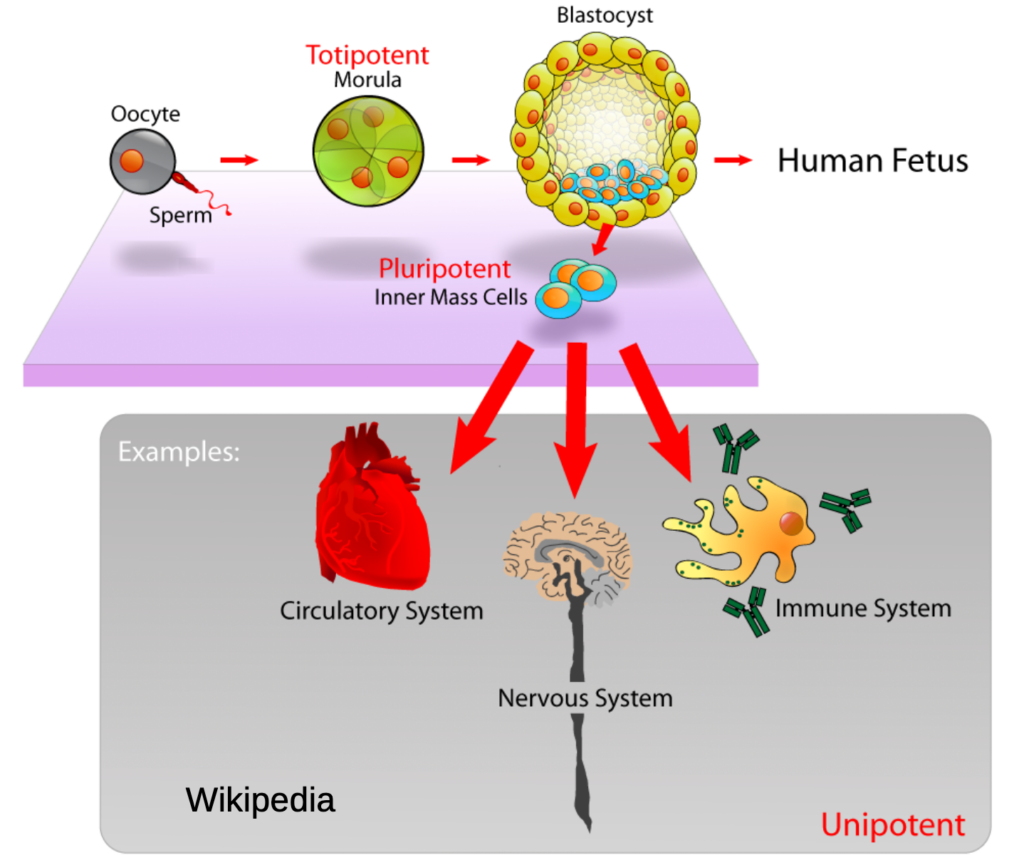
Après le jour 4, les cellules de l’embryon se spécialisent et perdent leur totipotence. Les cellules extérieures forment une membrane externe qui abrite des cellules souches embryonnaires internes.
Lorsqu’elles sont mises dans des boîtes de culture en laboratoire, ces cellules souches embryonnaires prolifèrent de façon illimitée pendant des années, pour générer des cellules filles identiques à elles mêmes. Si on modifie les conditions de culture, ces cellules souches embryonnaires peuvent générer chacun des 220 types cellulaires constituant notre organisme, y compris les cellules sexuelles. Pour cette raison elles sont appelées cellules souches pluripotentes.
Les premières lignées de cellules souches pluripotentes ont été obtenues chez l’homme en 19985.
Ces recherches sur les cellules souches embryonnaires sont très encadrées par les lois de bioéthique. Les embryons proviennent d’embryons générés dans les laboratoires de fécondation in vitro, après abandon du projet d’enfant et accord des parents. Chaque projet de recherche est autorisé par une agence réglementaire.
Si notre système immunitaire pouvait tolérer que l’on implante dans notre corps des cellules avec un patrimoine génétique différent, nous disposerions ainsi d’une source illimitée de cellules souches, capables de réparer des tissus et organes lésés de notre organisme. Mais notre système immunitaire ne tolère pas que l’on implante des cellules génétiquement différentes.
D’où, pour éviter les incompatibilités génétiques, l’énorme intérêt de pouvoir reprogrammer nos propres cellules en cellules souches pluripotentes aux propriétés identiques à celles des souches embryonnaires.
Une quasi immortalité est observée chez certaines espèces de notre planète.
Cette révolution conceptuelle de pouvoir générer pour tout individu une source illimitée de cellules souches pluripotentes n’est pas si surprenante si nous rappelons que la nature a déjà créé des espèces quasiment immortelles (voir Wikipedia). Une petite méduse d’environ 1 cm « Turritopsis dohrnii » est considérée comme immortelle. Cette petite méduse se retrouve en Méditerranée et dans la plupart des océans du globe. Si elle subit une lésion, est malade ou vieillit, elle revient aux premiers stades de sa vie, au stade d’un polype capable de générer toute une colonie de polypes puis de nouvelles méduses, et ceci infiniment.
Un autre animal quasiment immortel est le ver planaire, un petit ver plat aquatique de moins de 4 cm. Si vous le coupez en 279 morceaux, chacun des 279 morceaux répare les parties manquantes pour reconstituer un vers fonctionnel, soit 279 vers. Et vous pouvez répéter l’expérience en partant du même ver planaire pendant 15 ans. L’hydre, petit polype d’eau douce, a les mêmes capacités de régénération. Son nom lui a été donné parce que l’animal, après avoir la tête tranchée, voit une nouvelle tête lui repousser, un peu comme l’hydre de Lerne. N’importe quel fragment du corps comportant quelques centaines de cellules épithéliales peut régénérer l’animal entier. Un petit lézard, la salamandre, a également des capacités de réparation majeure : réparation d’un œil, d’une partie du coeur, d’une patte. D’autres espèces quasiment immortelles sont étudiées de façon approfondie pour comprendre les mécanismes sous jacents. Notamment le rat taupe nu doué d’une longévité exceptionnelle. J’y reviendrai en détail dans un prochain article.
Les mécanismes sous-jacents à cette immortalité/réparation sont proches de ceux trouvés par le Pr Yamanaka pour reprogrammer les cellules d’un individu adulte en cellules souches pluripotentes. Ils reposent sur des cellules souches. En cas de stress/lésion, les cellules adultes de ces espèces se dédifférencient en cellules souches, cellules jeunes capables de proliférer de façon massive et de générer soit des cellules souches filles identiques aux cellules souches mères, soit des cellules faisant fonctionner l’organisme : tube digestif, peau, œil, coeur, etc…
Et même chez des espèces développées comme l’être humain, certains tissus sont en constant renouvellement, grâce aux cellules souches adultes.
Prenons pour exemple notre sang. Les globules blancs de notre sang ne vivent qu’une journée, les plaquettes 7 jours, les globules rouges 120 jours. Chaque jour, un tout petit contingent de cellules souches, dites cellules souches hématopoïétiques, produit 400 milliards de cellules sanguines, soit environ 1 % de l’ensemble des cellules de notre corps !
Ces cellules souches hématopoïétiques sont dans la moelle osseuse. A la différence des cellules souches pluripotentes capables de générer chacun des 220 types de cellules de notre organisme, elles ne génèrent que les 9 types cellulaires présents dans notre sang. Ces cellules souches hématopoïétiques sont largement utilisées en thérapeutique depuis 40 ans (5000 greffes de cellules souches hématopoïétiques chaque année en France, essentiellement en cas de cancer). Et ayant mis en place en 1994 l’unité de thérapie cellulaire pour préparer ces cellules souches hématopoïétiques au CHU de Montpellier, je suis toujours émerveillé 30 ans après que la nature ait créé les mécanismes permettant de remplacer l’ensemble des cellules du sang et du système immunitaire d’un individu de 60 ans avec les cellules souches hématopoïétiques présentes dans le sang de cordon prélevé à la naissance d’un bébé compatible sur un plan génétique. Une vraie cure de jouvence pour les cellules du sang et immunitaires de ces patients !
Les cellules de nos cryptes intestinales sont également en constant renouvellement tous les 5 jours grâce aux cellules souches intestinales, notre peau tous les 21 jours du fait des cellules souches kératinocytaires, notre foie a aussi une grande capacité de réparation. Même nos os sont en constant renouvellement : 25 % de l’os spongieux (extrémité des os) et 5 % de l’os cortical grâce aux cellules souches mésenchymateuses sont renouvelés chaque année. Certains de nos tissus ou organes ne sont cependant quasiment pas renouvelés, les cellules du muscle cardiaque, les cellules des muscles intercostaux, les neurones. Mais ces concepts évoluent. Une étude récente basée sur des méthodes isotopiques et d’imagerie cellulaire a montré que nos organes contiennent une mosaïque de cellules, des cellules jeunes et des cellules très âgées, y compris les cellules des vaisseaux sanguins et du foie ou du pancréas connus comme étant fréquemment renouvelées6.
Alors, si nous avons déjà des cellules souches permettant le renouvellement de nos tissus, pourquoi vieillissons-nous ?
Plusieurs mécanismes élucidés ces 20 dernières années expliquent pourquoi nous vieillissons. Je listerai ici les deux principaux et je reviendrai sur cette question centrale dans un prochain article.
Une première raison est que nos cellules adultes ont une horloge interne – les télomères – limitant leur potentiel de division cellulaire à 50-70 divisions.
Les télomères (télomère provient du grec telos, la fin, et meros, partie = la partie à la fin du chromosome) sont constitués de séquences répétitives aux deux extrémités du chromosome. A chaque division, nos cellules adultes perdent une séquence répétitive télomèrique.
Et en fonction de la longueur des télomères restants, leur rythme de division se ralentit puis s’arrête vers 50-70 divisions (limite de Hayflick). Les cellules rentrent en sénescence et ne prolifèrent plus. Ce mécanisme explique en partie que notre limite d’âge est estimée à 120 ans. A la différence des cellules adultes, les cellules souches embryonnaires ne raccourcissent pas leurs télomères. Elles expriment une enzyme – la télomérase – permettant de resynthétiser les séquences répétitives lorsqu’elles se divisent. De même, la clef de reprogrammation de cellules adultes en cellules souches pluripotentes permet de faire exprimer l’enzyme télomérase qui va resynthétiser les séquences répétitives télomériques manquantes à l’extrémité des chromosomes. Un même mécanisme contribue à la relative immortalité des espèces listées ci-dessous : en cas de lésion ou stress, leurs cellules adultes se dédifférencient en cellules souches exprimant la télomérase. Etant donné l’importance de cette horloge interne contrôlant le nombre de divisions, une réexpression de la télomérase pourrait avoir un intérêt pour rajeunir nos cellules. Une limite est de stimuler la formation de cancers, les cellules tumorales exprimant la télomérase pour pouvoir proliférer. Un extrait de la plante Astragalus membranaceus, le TA65, issu de la médecine traditionnelle Chinoise stimule l’expression de la télomérase et a des effets bénéfiques chez la souris. Un premier essai thérapeutique chez des patients atteint d’un syndrome métabolique semble montrer des effets bénéfiques. Mais, soyons plus que prudent. Etant donné les convoitises commerciales et enjeux financiers, tout ceci mérite confirmation.
2. Une deuxième raison est que notre génome mute constamment. Chaque cellule subit en moyenne plusieurs centaines de mutations par jour. Ces mutations continues sont essentielles pour créer la diversité de la vie, la diversité des espèces vivantes. Rappelons que nous provenons tous de bactéries qui, par mutations, ont pu se diversifier en espèces pluricellulaires de plus en plus sophistiquées, dont l’être humain. Ces mutations sont induites par des erreurs lors de la réplication ou transcription de notre ADN, par les rayonnements, principalement le soleil, et par des molécules chimiques très réactives produites par nos cellules, principalement les dérivés réactifs de l’oxygène (ROS). Ces ROS à faible concentration sont essentielles pour la vie de nos cellules. En trop fortes concentrations, elles endommagent nos cellules.
Mais la nature a bien conçu notre organisme. Nos cellules possèdent de multiples systèmes de réparation permettant de corriger ces mutations. Si elles ne sont pas corrigées, la grande majorité de ces mutations conduit à une mort cellulaire ou une destruction par notre système immunitaire. Avec l’âge, ces mécanismes de réparation et notre système immunitaire sont moins efficaces entraînant une accumulation de mutations et une moindre capacité à proliférer de nos cellules. Dans certains cas, l’accumulation de ces mutations peut conduire à des cancers.
Cette année, je reviendrai plus en détail sur certains concepts, notamment les théories du vieillissement dans les différentes civilisations, les marqueurs et mécanismes de vieillissement, les applications cliniques de ces cellules souches pluripotentes.
Références
1. Induction of Pluripotent Stem Cells from Adult Human Fibroblasts by Defined Factors. Kazutoshi Takahashi, Koji Tanabe, Mari Ohnuki, Tomoko Ichisaka, Kiichiro Tomoda, Shinya Yamanaka. Cell. 2007 Nov 30;131(5):861-72. Télécharger le pdf.
2. Lapasset L., Milhavet O., Prieur A., Besnard E., Babled A., Aït-Hamou N., Leschik J., Pellestor F., Ramirez J.-M., De Vos J., et al. Rejuvenating senescent and centenarian human cells by reprogramming through the pluripotent state. Genes Dev. 2011;25:2248–2253. Télécharger le pdf.
3. Julia Deinsberger, David Reisinger and Benedikt Weber. Global trends in clinical trials involving pluripotent stem cells: a systematic multi-database analysis. Regenerative Medicine (2020) 5:15. Télécharger le pdf.
4. Sophie Arnaud-Haond, Carlos M. Duarte, Elena Diaz-Almela, Núria Marbà,Tomas Sintes, Ester A. Serrão. Implications of Extreme Life Span in Clonal Organisms: Millenary Clones in Meadows of the Threatened Seagrass Posidonia oceanica. Plos One. February 2012. Télécharger le pdf.
5. Thomson JA, Itskovitz-Eldor J, Shapiro SS, et al. (1998) Embryonic stem cell lines derived from human blastocysts. Science 282: 1145–1147.
6. Rafael Arrojo e Drigo, Varda Lev-Ram, Swati Tyagi, Ranjan Ramachandra, Thomas Deerinck, Eric Bushong, Sebastien Phan, Victoria Orphan, Claude Lechene, Mark H. Ellisman, and Martin W. Hetzer. Age Mosaicism across Multiple Scales in Adult Tissues. Cell Metabolism 30, 343–351, 2019. Télécharger le pdf.
Nos précédents Regards sur la science :
Le microbiote, cet ami essentiel à notre survie et pour communiquer avec notre environnement.
Pourquoi des Regards sur la Science sur le site ifym.fr?
Quand nos cerveaux se mettent sur la même longueur d’onde
Sommes nous seuls dans l’Univers?
